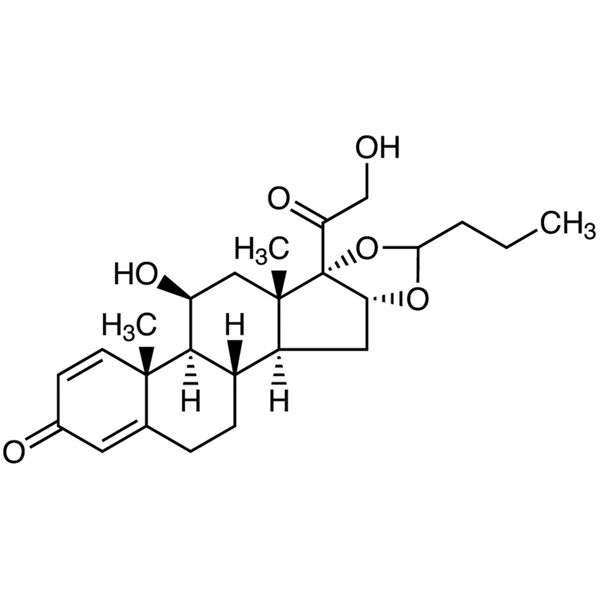
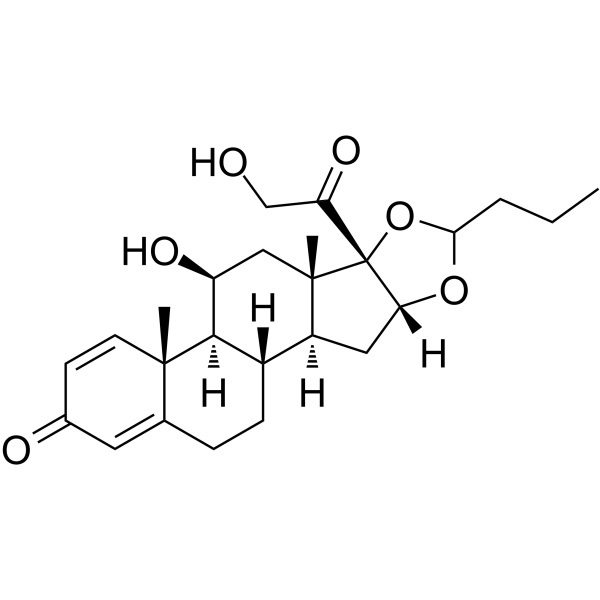
Budésonide CAS 51333-22-3 Analyse 98,0~102,0 %
Shanghai Ruifu Chemical Co., Ltd. est le principal fabricant de budésonide (CAS : 51333-22-3) de haute qualité. Ruifu Chemical peut fournir une livraison dans le monde entier, des prix compétitifs, un excellent service, des quantités petites et en vrac disponibles. Achetez du budésonide, Veuillez contacter : alvin@ruifuchem.com
| Nom chimique | Budésonide |
| Synonymes | (+)-16α,17α-Butylidènedioxy-11β,21-Dihydroxy-1,4-Prégnadiène-3,20-Dione ; 16,17-Butylidènebis(oxy)-11,21-Dihydroxypregna-1,4-Diène-3,20-Dione ; Rhinocorte ; Pulmicort; Entocort; Symbicort |
| État des stocks | En stock, production commerciale |
| Numéro CAS | 51333-22-3 |
| Formule moléculaire | C25H34O6 |
| Poids moléculaire | 430,54 g/mol |
| Point de fusion | 221,0 ~ 232,0 ℃ |
| Solubilité | Insoluble dans l'eau. Soluble dans le chloroforme, le méthanol. Légèrement soluble dans l'éthanol, l'acétone. Très légèrement soluble dans le dichlorométhane, l'éther |
| Certificat d'authenticité et fiche signalétique | Disponible |
| Origine du produit | Shanghai, Chine |
| Catégories de produits | API (Ingrédient Pharmaceutique Actif) |
| Attention | Non destiné à un usage humain. Pour usage de recherche uniquement. |
| Marque | Produit chimique Ruifu |
| Articles | Spécifications | Résultats |
| Apparence | Poudre cristalline blanche à blanc cassé | Poudre cristalline blanche |
| Dosage du budésonide | 98,0~102,0 % | 98,7% |
| Perte au séchage | <0,30% | 0,19% |
| Toute impureté unique | <0,20% | <0,20% |
| Épimère A | 40,0~51,0 % | 47,29% |
| Méthanol | <0,10% | 0,005% |
| Spectre infrarouge | Conforme à la structure | Conforme |
| Spectre RMN 1H | Conforme à la structure | Conforme |
| Conclusion | Le produit a été testé et est conforme aux spécifications données | |
Forfait : Bouteille, sac en papier d'aluminium, tambour de 25 kg/carton ou selon les exigences du client.
Conditions de stockage : Gardez le récipient bien fermé. Conserver dans un entrepôt frais, sec (2 ~ 8 ℃) et bien ventilé, à l'écart des substances incompatibles. Tenir à l'écart du soleil ; éviter le feu et les sources de chaleur ; éviter l'humidité.
Expédition :Livraison dans le monde entier par avion, par FedEx / DHL Express. Fournir une livraison rapide et fiable.
Budésonide
C25H34O6 430,53
Pregna-1,4-diène-3,20-dione, 16,17-[1R-butylidènebis(oxy)]-11,21-dihydroxy et pregna-1,4-diène-3,20-dione,16,17-[1S-butylidènebis(oxy)]-11,21-dihydroxy ;
(RS)-11,16,17,21-Tetrahydroxypregna-1,4-diène-3,20-dione cyclique 16,17-acétal avec butyraldéhyde [51372-29-3; 51372-28-2; 51333-22-3].
DÉFINITION
Modifier pour lire :
Le budésonide est un mélange de deux formes épimères, l'épimère A(C-22S) et l'épimère B(C-22R). Il contient 40,0 % de NLT (RB 1 - juin - 2011) et 51,0 % de NMT d'épimère A, et la somme des deux épimères est de 98,0 % de NLT et 102,0 % de NMT de C25H34O6, calculés sur la base séchée.
[Remarque-Protégez toutes les solutions contenant du budésonide de la lumière.]
IDENTIFICATION
• A. Absorption infrarouge <197K>
• B. Absorption ultraviolette<197U>
Solution échantillon : 25 µg/mL
Milieu : Méthanol
Critères d'acceptation : Répond aux exigences
ESSAI
Modifier pour lire :
• Procédure
Tampon : 3,17 mg/mL de phosphate de sodium monobasique et 0,23 mg/mL d'acide phosphorique. Le pH est de 3,2 ± 0,1.
Phase mobile : Acétonitrile et Tampon (32:68)
Solution standard : Dissoudre une quantité de Budésonide RS USP dans de l'acétonitrile et diluer quantitativement avec du tampon pour obtenir une solution ayant une concentration de 0,5 mg/mL, en maintenant la proportion d'acétonitrile dans cette solution à NMT 30 %.
Solution échantillon : Dissoudre 25 mg de budésonide dans 15 mL d'acétonitrile dans une fiole jaugée de 50 mL et diluer avec le tampon jusqu'au volume.
Système chromatographique
(Voir Chromatographie<621>, Adéquation du système.)
Mode : LC
Détecteur : UV 254 nm
Colonne : 4,6-mm × 15-cm ; 5-µm emballage L1
Débit : 1,5 mL/min
Taille de l'injection : 20 µL
Adéquation du système
Échantillon : Solution étalon
[Remarque-Le temps de rétention relatif de l'épimère A est de 1,1 par rapport à l'épimère B.]
Exigences d'aptitude
Résolution : NLT 1,5 entre les deux pics de l'épimère du budésonide
Efficacité de la colonne : plaques théoriques NLT 5500, déterminées à partir du pic de l'épimère B du budésonide
Analyse
Échantillons : solution standard et solution échantillon
Calculez le pourcentage d'épimère A (C25H34O6) dans la portion de Budésonide prélevée :
Résultat = [rUA/(rUA + rUB)] × 100
rUA = surface du pic de l'épimère A de la solution échantillon
rUB = surface du pic de l'épimère B de la solution échantillon
Calculez le pourcentage de C25H34O6 dans la portion de Budésonide prise :
Résultat = [(rUA + rUB)/(rSA + rSB)] × (CS/CU) × 100
rUA = surface du pic de l'épimère A de la solution échantillon
rUB = surface du pic de l'épimère B de la solution échantillon
rSA = aire du pic de l'épimère A de la solution étalon
rSB = aire du pic de l'épimère B de la solution étalon
CS = concentration de Budésonide RS USP dans la solution étalon (mg/mL)
CU = concentration de budésonide dans la solution échantillon (mg/mL)
Critères d'acceptation
Epimère A : 40,0 % (RB 1 - juin - 2011) - 51,0 % sur base séchée
Les deux épimères : 98,0 %-102,0 % sur base séchée
IMPURETÉS
• Procédure 1 : Limite de 21-Acétate de Budésonide
Tampon : 3,17 mg/mL de phosphate de sodium monobasique et 0,23 mg/mL d'acide phosphorique. Le pH est de 3,2 ± 0,1.
Phase mobile : Acétonitrile et Tampon (45:55)
Solution standard : Dissoudre une quantité de Budésonide RS USP dans de l'acétonitrile et diluer quantitativement avec du tampon pour obtenir une solution ayant une concentration de 0,5 mg/mL, en maintenant la proportion d'acétonitrile dans cette solution à NMT 30 %.
Solution échantillon : Dissoudre 25 mg de budésonide dans 15 mL d'acétonitrile dans une fiole jaugée de 50 mL et diluer avec le tampon jusqu'au volume.
Système chromatographique
(Voir Chromatographie<621>, Adéquation du système.)
Mode : LC
Détecteur : UV 254 nm
Colonne : 4,6-mm × 15-cm ; 5-µm emballage L1
Débit : 1,5 mL/min
Taille de l'injection : 20 µL
Adéquation du système
Échantillon : Solution étalon
[Remarque - Les temps de rétention relatifs pour le premier épimère élué du 21-acétate de budésonide, le deuxième épimère élué du 21-acétate de budésonide, le premier épimère élué du budésonide (épimère B) et le deuxième épimère élué du budésonide (épimère A) sont respectivement de 3,1, 3,2, 1,0 et 1,1. ]
Exigences d'aptitude
Efficacité de la colonne : plaques théoriques NLT 5500, déterminées à partir du pic de l'épimère B du budésonide
Analyse
Échantillon : Exemple de solution
Calculez le pourcentage de 21-acétate de budésonide dans la portion de budésonide prise :
Résultat = (rT1/rT2) × 100
rT1 = somme des aires des pics des deux épimères du 21-acétate de budésonide
rT2 = somme des aires des deux pics de budésonide
Critères d'acceptation : NMT On retrouve 0,10% du 21-acétate de budésonide.
• Procédure 2 : Limite de 11-Kétobudésonide
Tampon : 3,17 mg/mL de phosphate de sodium monobasique et 0,23 mg/mL d'acide phosphorique. Le pH est de 3,2 ± 0,1.
Phase mobile : acétonitrile, isopropanol et tampon (26:9:65)
Solution standard : Dissoudre une quantité de Budésonide RS USP dans de l'acétonitrile et diluer quantitativement avec du tampon pour obtenir une solution ayant une concentration de 0,5 mg/mL, en maintenant la proportion d'acétonitrile dans cette solution à NMT 30 %.
Solution échantillon : Dissoudre 25 mg de budésonide dans 15 mL d'acétonitrile dans une fiole jaugée de 50 mL et diluer avec le tampon jusqu'au volume.
Système chromatographique
(Voir Chromatographie<621>, Adéquation du système.)
Mode : LC
Détecteur : UV 254 nm
Colonne : 4,6-mm × 15-cm ; 3,5-µm emballage L1
Température de la colonne : 50
[Remarque-Préchauffez la phase Mobile à 50.]
Débit : 1,5 mL/min
Taille de l'injection : 20 µL
Adéquation du système
Échantillon : Solution étalon
[Remarque - Les temps de rétention relatifs pour les deux épimères du 11-cétobudésonide sont respectivement de 0,73 et 0,78 ; les temps de rétention relatifs pour le 21-déhydrobudésonide, le 14,15-déhydrobudésonide et le premier épimère élué du budésonide (épimère B) sont respectivement de 0,68, 0,84 et 1,0.]
Exigences d'aptitude
Efficacité de la colonne : plaques théoriques NLT 5500, déterminées à partir du pic de l'épimère B du budésonide
Analyse
Échantillon : Exemple de solution
Calculez le pourcentage de 11-cétobudésonide dans la portion de budésonide prise :
Résultat = (rT1/rT2) × 100
rT1 = somme des aires des pics des deux pics du kétobudésonide
rT2 = somme des aires des deux pics de budésonide
Critères d'acceptation : NMT 0,2 % de 11-cétobudésonide est trouvé.
• Procédure 3
Tampon : 3,17 mg/mL de phosphate de sodium monobasique et 0,23 mg/mL d'acide phosphorique. Le pH est de 3,2 ± 0,1.
Phase mobile : Acétonitrile et Tampon (32:68)
Solution standard : Dissoudre une quantité de Budésonide RS USP dans de l'acétonitrile et diluer quantitativement avec du tampon pour obtenir une solution ayant une concentration de 0,5 mg/mL, en maintenant la proportion d'acétonitrile dans cette solution à NMT 30 %.
Solution échantillon : Dissoudre 25 mg de budésonide dans 15 mL d'acétonitrile dans une fiole jaugée de 50 mL et diluer avec le tampon jusqu'au volume.
Système chromatographique
(Voir Chromatographie<621>, Adéquation du système.)
Mode : LC
Détecteur : UV 254 nm
Colonne : 4,6-mm × 15-cm ; 5-µm emballage L1
Débit : 1,5 mL/min
Taille de l'injection : 20 µL
Adéquation du système
Échantillon : Solution étalon
Exigences d'aptitude
Efficacité de la colonne : plaques théoriques NLT 5500, déterminées à partir du pic de l'épimère B du budésonide
Analyse
Échantillon : Exemple de solution
Calculez le pourcentage de chaque impureté dans la portion de budésonide prise :
Résultat = (rU/rT) × 100
rU = surface du pic pour chaque impureté
rT = somme des aires de tous les pics
Critères d'acceptation : Voir le tableau 1.
Tableau 1 Nom Critères d'acceptation du temps de rétention relatif, NMT (%)
16-Hydroxyprednisolonea 0,11 0,2
d-Homobudésonideb 0,36 0,10
21-Déhydrobudésonide (épimères)c 0,61 ; 0,66 0,07d
14,15-Déhydrobudésonidée 0,86 0,10
Total des impuretés spécifiées - 0,4f
Toute autre impureté individuelle - 0,10
Impuretés totales non précisées - 0,4
a 11,16,17,21-Tetrahydroxypregna-1,4-diène-3,20-dione.
b 16,17-[(1RS)-Butylidènebis(oxy)]-11-hydroxy-17-(hydroxyméthyl)-d-homoandrosta-1,4-diène-3,17a-dione.
c 16,17-[(1RS)-Butylidènebis(oxy)]-11-hydroxy-3,20-dioxopregna-1,4-dien-21-al.
d La limite inclut les deux épimères.
e 16,17-[(1RS)-Butylidènebis(oxy)]-11,21-dihydroxypregna-1,4,14-triène-3,20-dione.
f Le total des impuretés spécifiées comprend le 11-kétobudénoside obtenu lors du test pour la limite de 11-kétobudénoside et les impuretés énumérées ci-dessus.
TESTS SPÉCIFIQUES
• Tests de dénombrement microbien<61>et tests pour les micro-organismes spécifiés<62> : le nombre total de micro-organismes aérobies est de NMT 103 ufc/g, et le nombre total combiné de moisissures et de levures est de NMT 102 ufc/g.
• Perte au séchage<731> : Sécher un échantillon à 105 à poids constant : il perd NMT 0,3% de son poids.
EXIGENCES SUPPLÉMENTAIRES
• Conditionnement et stockage : Conserver dans des contenants étanches et résistants à la lumière. Conserver à température ambiante contrôlée.
• Normes de référence USP<11>
USP Budésonide RS
Comment acheter ? Veuillez contacterDr Alvin Huang : sales@ruifuchem.com ou alvin@ruifuchem.com
15 ans d'expérience ?Nous avons plus de 15 ans d'expérience dans la fabrication et l'exportation d'une large gamme d'intermédiaires pharmaceutiques ou de produits chimiques fins de haute qualité.
Principaux marchés ? Vendre sur le marché intérieur, en Amérique du Nord, en Europe, en Inde, en Corée, au Japon, en Australie, etc.
Avantages ? Qualité supérieure, prix abordable, services professionnels et support technique, livraison rapide.
Qualité Assurance? Système de contrôle de qualité strict. Les équipements professionnels d'analyse comprennent RMN, LC-MS, GC, HPLC, ICP-MS, UV, IR, OR, K.F, ROI, LOD, MP, clarté, solubilité, test de limite microbienne, etc.
Échantillons? La plupart des produits fournissent des échantillons gratuits pour l'évaluation de la qualité, les frais d'expédition doivent être payés par les clients.
Audit d'usine? Audit d'usine bienvenu. Veuillez prendre rendez-vous à l'avance.
QUANTITÉ MINIMALE DE COMMANDE ? Aucun MOQ. La petite commande est acceptable.
Délai de livraison? Si en stock, livraison sous trois jours garantie.
Transport? Par Express (FedEx, DHL), par Air, par Mer.
Des documents ? Service après-vente : COA, MOA, ROS, MSDS, etc. peuvent être fournis.
Synthèse personnalisée? Peut fournir des services de synthèse personnalisés pour répondre au mieux à vos besoins de recherche.
Conditions de paiement? La facture pro forma sera envoyée en priorité après confirmation de la commande, accompagnée de nos coordonnées bancaires. Paiement par T/T (Transfert Télex), PayPal, Western Union, etc.
Symboles de danger Xn - Nocif
Codes de risque R40 - Preuve limitée d'un effet cancérigène
R36/37/38 - Irritant pour les yeux, les voies respiratoires et la peau.
R20/21/22 - Nocif par inhalation, par contact avec la peau et par ingestion.
Description de sécurité S22 - Ne respirez pas la poussière.
S36 - Portez des vêtements de protection appropriés.
S26 - En cas de contact avec les yeux, rincer immédiatement et abondamment à l'eau et consulter un médecin.
WGK Allemagne 3
RTECSTU3723000
Code SH 2937 2900.99
Le budésonide (CAS : 51333-22-3) (nom de marque : Pulmicort) est un corticostéroïde synthétique. Le budésonide est indiqué pour le traitement d'entretien et prophylactique de l'asthme. Il est également utilisé pour la gestion à long terme de la maladie pulmonaire obstructive chronique (MPOC). Le budésonide est également utile pour le traitement des maladies inflammatoires de l’intestin, notamment la maladie de Crohn, la colite ulcéreuse et la colite microscopique, ainsi que pour le traitement de la rhinite allergique. Le budésonide présente une puissante activité glucocorticoïde et une faible activité minéralocorticoïde in vivo. Il est efficace pour inhiber les activités de plusieurs types de cellules et médiateurs participant à l'inflammation à médiation allergique ou non allergique.
Le budésonide est un médicament clinique couramment utilisé dans le traitement de l'asthme bronchique en Chine. Il peut être utilisé pour l'asthme non hormono-dépendant ou hormono-dépendant et pour la bronchite asthmatique chronique. Ou bien, il est utilisé pour le traitement de la rhinite allergique saisonnière et de la rhinite allergique survenant depuis de nombreuses années et il est utilisé pour prévenir la régénération des polypes après l'ablation des polypes nasaux.