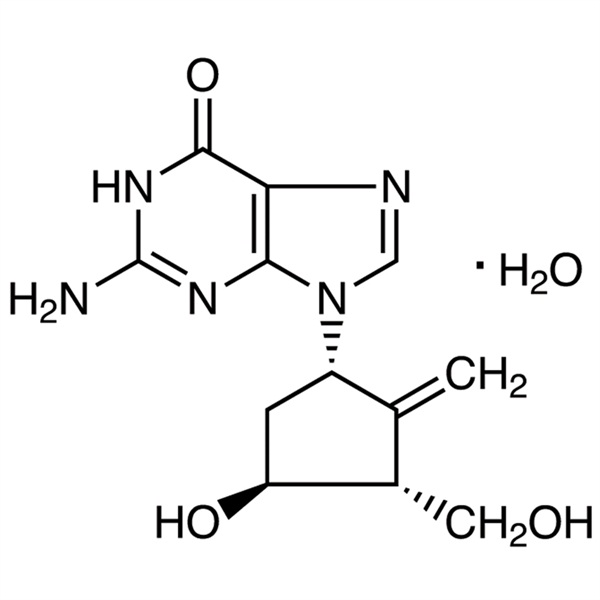
Entécavir monohydraté CAS 209216-23-9 Analyse 98,0 % ~ 102,0 % API USP EP Standard Antiviral Infection antivirale par l'hépatite B
Ruifu Chemical est le principal fournisseur de monohydrate d'entécavir (CAS : 209216-23-9) de haute qualité, pouvant répondre à la norme USP/EP , utilisé dans le traitement de l'infection par l'hépatite B.
Ruifu fournit des API et des intermédiaires pharmaceutiques depuis plus de 15 ans.
Ruifu Chemical peut fournir une livraison dans le monde entier, des prix compétitifs et un excellent service.
Achetez du monohydrate d'entécavir, veuillez nous contacter par e-mail : alvin@ruifuchem.com
| Nom chimique | Entécavir monohydraté |
| Synonymes | Entécavir hydraté ; 9-[(1S,3R,4S)-4-Hydroxy-3-(hydroxyméthyl)-2-méthylènecyclopentyl]guanine monohydraté |
| Numéro CAS | 209216-23-9 |
| État des stocks | En stock, production pouvant atteindre des tonnes |
| Formule moléculaire | C12H17N5O4 |
| Poids moléculaire | 295.3 |
| Point de fusion | >220 ℃ |
| Densité | 1,81 |
| Conditions d'expédition | Expédié à température ambiante |
| Certificat d'authenticité et fiche signalétique | Disponible |
| Origine du produit | Shanghai, Chine |
| Catégories de produits | API (Ingrédient Pharmaceutique Actif) |
| Marque | Produit chimique Ruifu |
| Article | Spécifications |
| Apparence | Poudre cristalline blanche ou presque blanche |
| Solubilité | Librement soluble dans le diméthylformamide, légèrement soluble dans l'eau, l'éthanol et le méthanol |
| Identification IR | Le spectre de l'échantillon correspond à celui de l'étalon de référence |
| Identification HPLC | Le temps de rétention de l'échantillon à tester correspond à celui de l'étalon de référence |
| Teneur en eau (par K.F) | 5,5% ~ 6,5% |
| Rotation optique spécifique | +24,0° à +30,0° (DMF : MeOH=1:1 C=1%) (sur substance anhydre) |
| Résidus à l'allumage | ≤0,10 % |
| Substances associées | |
| Furoentécavir | ≤0,10 % |
| Entécavir 1-Épimère | ≤0,10 % |
| Entécavir 3-Épimère | ≤0,10 % |
| 8-Hydroxy-Entécavir | ≤0,10 % |
| Entécavir 4-Épimère | ≤0,10 % |
| 8-Méthoxy Entécavir | ≤0,10 % |
| 4-Diméthylsilyl Entécavir | ≤0,10 % |
| Composé A lié à l’entécavir | ≤0,10 % |
| Toute impureté non spécifiée | ≤0,10 % |
| Impuretés totales | ≤0,30% |
| Solvants résiduels | |
| Méthanol | ≤600 ppm |
| Dichlorométhane | ≤300 ppm |
| Acétate d'éthyle | ≤1000ppm |
| Tétrahydrofurane | ≤720 ppm |
| Toluène | ≤890 ppm |
| Chlorure de benzyle | ≤1000ppm |
| Alcool benzylique | ≤1000ppm |
| Limite microbienne | |
| Comptes aérobies totaux | ≤100 ufc/g |
| Levures et moisissures | ≤10 ufc/g |
| Escherichia coli | Ne devrait pas être détecté |
| Métaux lourds | ≤10 ppm |
| Dosage | 98,0 % ~ 102,0 % (HPLC ; sur une base anhydre) |
| Taille des particules | 95 % des particules doivent être inférieures à 125 μm |
| Norme de test | Norme d'entreprise ; Norme de la Pharmacopée des États-Unis (USP) |
| Utilisation | Médicament antiviral utilisé dans le traitement de l'infection par l'hépatite B |
Forfait : Bouteille, sac en papier d'aluminium, fût de 25 kg/carton ou selon les exigences du client.
Conditions de stockage : Gardez le récipient bien fermé. Conserver dans un entrepôt frais, sec (2-15℃) et bien ventilé, à l'écart des substances incompatibles. Tenir à l'écart du soleil ; éviter le feu et les sources de chaleur ; éviter l'humidité.
Expédition : Livrez dans le monde entier par avion, par mer, par FedEx / DHL Express. Fournir une livraison rapide et fiable.

| Description de la sécurité | 24/25 - Évitez tout contact avec la peau et les yeux. |
| Code SH | 2933990099 |
L'entécavir monohydraté (CAS 209216-23-9) est un médicament antiviral oral utilisé dans le traitement de l'infection par le virus de l'hépatite B (VHB). L'entécavir monohydraté est un analogue nucléosidique (plus précisément un analogue de la guanine) qui inhibe la transcription inverse, la réplication de l'ADN et la transcription dans le virus. Il s'agit d'un nouveau type de médicaments anti-virus de l'hépatite B à base de cyclopentyl acyl guanosine avec ses effets pharmacologiques similaires à ceux de l'entécavir. Il est cliniquement appliqué au traitement de l'hépatite B chronique chez l'adulte dans laquelle il existe une réplication virale active, une augmentation des transaminases sériques ALT ou des lésions actives montrées par l'histologie hépatique. L'entécavir monohydraté est un inhibiteur puissant et sélectif du VHB, avec une CE50 de 3,75 nM dans les cellules HepG2. L'entécavir est un inhibiteur de la transcriptase inverse. Il empêche le virus de l'hépatite B (VHB) de se multiplier et réduit la quantité de virus dans le corps.
Entécavir
C12H15N5O3·H2O 295,29
6H-Purin-6-one, 2-amino-1,9-dihydro-9-[(1S,3R,4S)-4-hydroxy-3-(hydroxymethyl)-2-méthylènecyclopentyl]-, monohydraté ;
9-[(1S,3R,4S)-4-Hydroxy-3-(hydroxyméthyl)-2-méthylènecyclopentyl]guanine monohydraté [209216-23-9] ; UNII : 5968Y6H45M.
Anhydre 277,28
DÉFINITION
L'entécavir est un monohydrate et contient 98 % de NLT et 102 % de NMT d'entécavir (C12H15N5O3), calculés sur une base anhydre.
IDENTIFICATION
Modifier pour lire :
• A. TESTS D'IDENTIFICATION SPECTROSCOPIQUE<197>, Spectroscopie Infrarouge : 197A ou 197K (CN 1-Mai-2020)
• B. Le temps de rétention du pic principal de la solution échantillon correspond à celui de la solution standard, tel qu'obtenu dans le test.
ESSAI
• PROCÉDURE
Solution A : Acétonitrile et eau (3:97)
Solution B : Acétonitrile
Phase mobile : voir le tableau 1. [REMARQUE- Les temps d'élution en gradient sont établis sur un système HPLC avec un volume de séjour d'environ 1,0 mL.]
Tableau 1 Temps (min) Solution A (%) Solution B (%)
0 100 0
8 100 0
50 77 23
75 17 83
90 100 0
100 100 0
Solution mère d’adéquation du système : 1,0 mg/mL de mélange d’adéquation du système USP Entecavir RS dans du méthanol
Solution d'adéquation du système : 0,2 mg/mL de mélange d'adéquation du système USP Entecavir RS dans la solution A à partir de la solution mère d'adéquation du système
Solution mère étalon : 1,0 mg/mL d’USP Entecavir Monohydrate RS dans du méthanol. Faire soniquer au besoin.
Solution étalon : 0,2 mg/mL d'USP Entecavir Monohydrate RS dans la solution A à partir de la solution mère étalon
Exemple de solution mère : 1,0 mg/mL d’Entécavir dans du méthanol. Faire soniquer au besoin.
Solution échantillon : 0,2 mg/mL d’entécavir dans la solution A à partir de la solution mère échantillon
Système chromatographique
(Voir Chromatographie<621>, Adéquation du système.)
Mode : LC
Détecteur : UV 254 nm
Colonne : 4,6-mm × 25-cm ; 5-µm emballage L1
Débit : 1 mL/min
Volume d'injection : 10 µL
Adéquation du système
Exemples : solution d'adéquation du système et solution standard
[ REMARQUE - Voir le tableau 2 pour les temps de rétention relatifs des composants dans la solution d'adéquation du système.]
Exigences d'aptitude
Résolution : NLT 3,5 entre l'entécavir 1-épimère et l'entécavir ; NLT 2.0 entre l'entécavir et le 8-hydroxy entécavir, système
solution adaptée
Facteur de queue : 0,8-1,5 pour l'entécavir, solution d'adéquation du système
Écart type relatif : NMT 1,5 %, solution standard
Analyse
Échantillons : solution standard et solution échantillon
Calculez le pourcentage d'entecavir (C12H15N5O3) dans la portion d'Entecavir prise :
Résultat = (ru /rs ) × (Cs /Cu ) × 100
ru = réponse maximale de l'entécavir à partir de la solution échantillon
rs = réponse maximale de l'entécavir de la solution étalon
Cs = concentration d'USP Entecavir Monohydrate RS dans la solution étalon (mg/mL)
Cu = concentration d'entécavir dans la solution échantillon (mg/mL)
Critères d'acceptation : 98%-102% sur base anhydre
IMPURETÉS
• IMPURETÉS ORGANIQUES
Solution A, Solution B, Phase mobile, Solution mère d'adéquation du système, Solution d'adéquation du système, Solution mère d'échantillon, Solution d'échantillon et Système chromatographique : procédez comme indiqué dans le test.
Solution mère étalon : utilisez la solution étalon du test.
Solution étalon : 0,2 µg/mL d'USP Entecavir Monohydrate RS dans la solution A à partir de la solution mère étalon
Adéquation du système
Exemples : solution d'adéquation du système et solution standard
[ REMARQUE - Voir le tableau 2 pour les temps de rétention relatifs des composants dans la solution d'adéquation du système.]
Exigences d'aptitude
Résolution : NLT 3,5 entre l'entécavir 1-épimère et l'entécavir ; NLT 2.0 entre l'entécavir et le 8-hydroxy entécavir, solution d'adéquation du système
Facteur de queue : 0,8-1,5 pour l'entécavir, solution d'adéquation du système
Écart type relatif : NMT 10,0 %, solution standard
Analyse
Échantillons : solution échantillon et solution standard
Calculez le pourcentage de chaque impureté dans la portion d'Entecavir prise :
Résultat = (ru /rs ) × (Cs /Cu ) × (1/F) × 100
ru = réponse maximale de chaque impureté de la solution échantillon
rs = réponse maximale de l'entécavir de la solution étalon
Cs = concentration d'USP Entecavir Monohydrate RS dans la solution étalon (mg/mL)
Cu = concentration d'entécavir dans la solution échantillon (mg/mL)
F = facteur de réponse relatif (voir tableau 2)
Critères d'acceptation : Voir le tableau 2. Ne pas tenir compte de tout pic inférieur à 0,05 %.
Tableau 2
Nom Temps de rétention relatif Facteur de réponse relatif Critères d’acceptation, NMT (%)
Furoentécavir a 0,73 1,0 0,1
Entécavir 1-épimère b 0,93 1,0 0,1
Entécavir 3-épimère c 0,96 1,0 0,1
Entécavir 1.0 - -
8-Hydroxy entécavir d 1,03 0,67 0,1
Entécavir 4-épimère e 1,08 1,0 0,1
8-Méthoxy entécavir f 1,27 0,67 0,1
4-Diméthylsilyl entécavir g 1,84 1,0 0,1
Composé apparenté à l'entécavir A 3.41 - -
Toute impureté non précisée - 1,0 0,1
Impuretés totales i - - 0,3
une 9-[(3aS,4S,6S,6aR)-3a,6-Dihydroxyhexahydro-1H-cyclopenta[c]furan-4-yl]guanine.
b 9-[(1R,3R,4S)-4-Hydroxy-3-(hydroxyméthyl)-2-méthylènecyclopentyl]guanine.
c 9-[(1S,3S,4S)-4-Hydroxy-3-(hydroxyméthyl)-2-méthylènecyclopentyl]guanine.
d 8-Hydroxy-9-[(1S,3R,4S)-4-hydroxy-3-(hydroxyméthyl)-2-méthylènecyclopentyl]guanine.
e 9-[(1S,3R,4R)-4-Hydroxy-3-(hydroxyméthyl)-2-méthylènecyclopentyl]guanine.
f 8-Méthoxy-9-[(1S,3R,4S)-4-hydroxy-3-(hydroxyméthyl)-2-méthylènecyclopentyl]guanine.
g 9-[(1S,3R,4S)-4-Hydroxydiméthylsilyl-3-(hydroxyméthyl)-2-méthylènecyclopentyl]guanine.
h Pour information seulement ; quantifié dans le test pour la limite du composé A apparenté à l'entécavir.
i Comprend la somme de toutes les impuretés trouvées dans les tests de limite du composé A associé à l'entécavir et des impuretés organiques.
• LIMITE DU COMPOSÉ A ASSOCIÉ À L'ENTÉCAVIR
Solution A : 0,1 % (v/v) d'acide trifluoroacétique dans l'eau
Solution B : 0,1 % (v/v) d'acide trifluoroacétique dans de l'acétonitrile
Phase mobile : voir le tableau 3. [ REMARQUE- Les temps d'élution en gradient sont établis sur un système HPLC avec un volume de séjour de
environ 1,0 ml.]
Tableau 3
Temps (min) Solution A (%) Solution B (%)
0 65 35
8 53 47
8,1 65 35
11 65 35
Solution étalon : 2 µg/mL de composé apparenté A RS USP à l'entécavir dans du méthanol
Solution échantillon : 1,0 mg/mL d’Entecavir dans du méthanol. Faire soniquer au besoin.
Système chromatographique
(Voir Chromatographie<621>, Adéquation du système.)
Mode : LC
Détecteur : UV 254 nm
Colonne : 4,6-mm × 5-cm ; 5-µm emballage L1
Températures
Échantillonneur automatique : 4°
Colonne : 30°
Débit : 2 mL/min
Volume d'injection : 10 µL
Adéquation du système
Échantillon : Solution étalon
Exigences d'aptitude
Facteur de queue : 0,8-1,5
Écart type relatif : NMT 3,0 %
Analyse
Échantillons : solution standard et solution échantillon
Calculez le pourcentage de composé A lié à l'entécavir dans la portion d'entécavir prise :
Résultat = (ru /rs ) × (Cs /Cu ) × 100
ru = réponse maximale du composé A lié à l'entécavir à partir de la solution échantillon
rs = réponse maximale du composé A apparenté à l'entécavir de la solution étalon
Cs = concentration du composé apparenté A RS de l'USP Entécavir dans la solution étalon (mg/mL)
Cu = concentration d'entécavir dans la solution échantillon (mg/mL)
Critères d'acceptation : NMT 0,1 %
TESTS SPÉCIFIQUES
• DÉTERMINATION DE L'EAU<921>, Méthode I, Méthode Ic : 5,5 %-7,0 %
• ROTATION OPTIQUE<781S>, Procédures, Rotation Spécifique
Solution échantillon : 10 mg/mL d'Entecavir dans un mélange de diméthylformamide et de méthanol (50:50)
Critères d'acceptation : +24° à +30°
EXIGENCES SUPPLÉMENTAIRES
• CONDITIONNEMENT ET CONSERVATION : Conserver dans des récipients bien fermés, à l'abri de la lumière. Conserver à température ambiante.
• NORMES DE RÉFÉRENCE USP<11>
USP Entécavir monohydraté RS
USP Composé apparenté à l'entécavir A RS
3-Benzyl-4-silyl entécavir ;
9-[(1S,3R,4S)-4-Diméthylphénylsilyl-3-(benzyloxyméthyl)-2-méthylènecyclopentyl]guanine.
C27H31N5O2Si 485,65
USP Entecavir Adéquation du système Mélange RS
Le mélange contient du monohydrate d'entécavir et les impuretés suivantes (d'autres impuretés peuvent également être présentes) :
Entécavir 1-épimère.
8-Hydroxy entécavir.
8-Méthoxy entécavir.