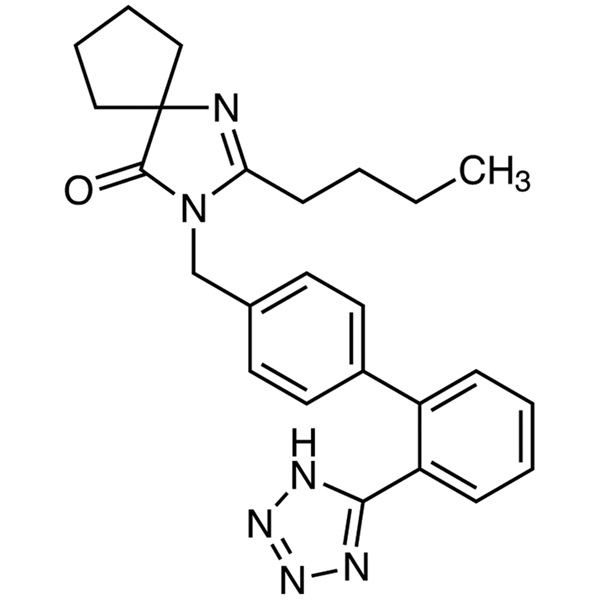
Irbésartan CAS 138402-11-6 Analyse 98,0~102,0 % (HPLC) Antihypertenseur standard API USP
Ruifu Chemical est le principal fournisseur d'irbésartan (CAS : 138402-11-6) de haute qualité, pouvant répondre à la norme USP. Ruifu Chemical fournit des API et des intermédiaires pharmaceutiques depuis plus de 15 ans.
Ruifu Chemical peut fournir une livraison dans le monde entier, des prix compétitifs et un excellent service.
Acheter de l'irbésartan et des intermédiaires associés, veuillez nous contacter par e-mail : alvin@ruifuchem.com
| Nom chimique | Irbésartan |
| Synonymes | BMS-186295 ; SR-47436 ; Aprovel ; Avapro ; 2-Butyl-3-[[2′-(1H-tétrazol-5-yl)[1,1′-biphényl]-4-yl]méthyl]-1,3-diazaspiro[4.4]non-1-en-4-one ; 2-Butyl-3-[[4-[2-(2H-tétrazol-5-yl)phényl]phényl]méthyl]-1,3-diazaspiro[4.4]non-1-en-4-one |
| Numéro CAS | 138402-11-6 |
| État des stocks | En stock, production pouvant atteindre des tonnes |
| Formule moléculaire | C25H28N6O |
| Poids moléculaire | 428,54 |
| Densité | 1,30 ± 0,10 g/cm3 |
| Point de fusion | 184,0 à 188,0℃ |
| Solubilité dans l'eau | Insoluble dans l'eau |
| Certificat d'authenticité et fiche signalétique | Disponible |
| Température de stockage | Conserver à long terme à 2-8 ℃ |
| Origine du produit | Shanghai, Chine |
| Catégories de produits | API (Ingrédient Pharmaceutique Actif) |
| Marque | Produit chimique Ruifu |
| Éléments de test | Spécifications | Résultats |
| Apparence | Poudre cristalline blanche à presque blanche | Poudre cristalline blanche |
| Identification | ||
| IR | Doit être conforme à la norme de référence | Conforme |
| HPLC | Doit être conforme à la norme de référence | Conforme |
| Teneur en eau (par K.F) | ≤0,50% | 0,15% |
| Cendres sulfatées | ≤0,20% | <0,20% |
| Méats lourds | ≤0,002% | <0,002% |
| Limite d'azide | ≤10 ppm | <10 ppm |
| Impuretés organiques | ||
| Composés A apparentés à l’irbésartan | ≤0,20% | 0,002% |
| Toute autre impureté individuelle | ≤0,10 % | 0,004% |
| Impuretés totales | ≤0,50 % (hors R-Isomère) | 0,33% |
| Solvants résiduels | ||
| Éthanol | ≤5000 ppm | 28 ppm |
| Dichlorométhane | ≤600 ppm | Non détecté |
| N,N-Diméthylformamide | ≤880 ppm | Non détecté |
| t-Éther butylméthylique | ≤5000 ppm | Non détecté |
| Xylène | ≤1500ppm | 320 ppm |
| Toluène | ≤890 ppm | Non détecté |
| Dosage (HPLC) | 98,0 ~ 102,0 % d'irbésartan (C25H28N6O), calculé sur une base anhydre | 99,9% |
| Conclusion | Le produit a été testé et est conforme à la norme USP 36. | |
Forfait : Bouteille, sac en papier d'aluminium, fût de 25 kg/carton ou selon les exigences du client.
Conditions de stockage : Gardez le récipient bien fermé. Conserver dans un entrepôt frais, sec (2-8℃) et bien ventilé, à l'écart des substances incompatibles. Tenir à l'écart du soleil ; éviter le feu et les sources de chaleur ; éviter l'humidité.
Expédition : Livrez dans le monde entier par avion, par mer, par FedEx / DHL Express. Fournir une livraison rapide et fiable.

Symboles de danger Xn - Nocif
Codes de risque 22 - Nocif en cas d'ingestion
Description de la sécurité
S26 - En cas de contact avec les yeux, rincer immédiatement et abondamment à l'eau et consulter un médecin.
S24/25 - Évitez tout contact avec la peau et les yeux.
WGK Allemagne 3
RTECSHM2950270
Code SH 2933290090
L'irbésartan (CAS : 138402-11-6) est un antagoniste des récepteurs de l'angiotensine II utilisé principalement pour le traitement de l'hypertension. L'irbésartan a été développé par Sanofi Research (qui fait désormais partie de Sanofi-Aventis). Il est commercialisé conjointement par Sanofi-Aventis et Bristol-Myers Squibb sous les noms commerciaux Aprovel, Karvea et Avapro. L'irbésartan est utilisé pour traiter l'hypertension artérielle. Avapro a été lancé en Allemagne, au Royaume-Uni et aux États-Unis pour le traitement de l'hypertension. Comme tous les antagonistes des récepteurs de l'angiotensine II, l'irbésartan est indiqué dans le traitement de l'hypertension.
L'irbésartan peut également retarder la progression de la néphropathie diabétique et est également indiqué pour réduire la progression de la maladie rénale chez les patients atteints de diabète de type 2, d'hypertension et de microalbuminurie (> 30 mg/24 heures) ou de protéinurie. L'irbésartan peut également réduire le remodelage électrique du myocarde, réduisant ainsi le taux de mortalité des patients souffrant d'hypertension. C'est le médicament le plus efficace pour le traitement de l'hypertension et des maladies cardiovasculaires.
Irbésartan
C25H28N6O 428,53
1,3-Diazaspiro[4.4]non-1-en-4-one, 2-butyl-3-[[2′-(1H-tétrazol-5-yl)[1,1′-biphényl]-4-yl]méthyl]-;
2-Butyl-3-[p-(o-1H-tétrazol-5-ylphényl)benzyl]-1,3-diazaspiro[4.4]non-1-en-4-one [138402-11-6]; UNII : J0E2756Z7N.
DÉFINITION
L'irbésartan contient 98,0 % de NLT et 102,0 % de NMT d'irbésartan (C25H28N6O), calculés sur une base anhydre.
IDENTIFICATION
Modifier pour lire :
• A. TESTS D'IDENTIFICATION SPECTROSCOPIQUE<197>, Spectroscopie Infrarouge : 197K (CN 1-MAI-2020)
• B. Le temps de rétention du pic principal de la solution échantillon correspond à celui de la solution standard, tel qu'obtenu dans le test.
ESSAI
• PROCÉDURE
Tampon : Acide phosphorique et eau (v/v) (5,5:950). Ajuster avec de la triéthylamine à un pH de 3,2.
Phase mobile : Acétonitrile et Tampon (330:670)
Solution d'adéquation du système : 0,05 mg/mL de chacun de USP Irbesartan RS et USP Irbesartan Related Composé A RS dans du méthanol
Solution étalon : 0,5 mg/mL d'USP Irbesartan RS dans du méthanol
Solution échantillon : 0,5 mg/mL d’irbésartan dans du méthanol
Système chromatographique
(Voir Chromatographie<621>, Adéquation du système.)
Mode : LC
Détecteur : UV 220 nm
Colonne : 4,0-mm × 25-cm ; emballage L1
Débit : 1 mL/min
Volume d'injection : 10 µL
Adéquation du système
Exemples : solution d'adéquation du système et solution standard
[ REMARQUE - Les temps de rétention relatifs pour le composé A apparenté à l'irbésartan et l'irbésartan sont respectivement de 0,8 et 1,0.]
Exigences d'aptitude
Résolution : NLT 2.0 entre l'irbésartan et le composé A apparenté à l'irbésartan, solution d'adéquation du système
Écart type relatif : NMT 1,0 %, solution standard
Analyse
Échantillons : solution standard et solution échantillon
Calculez le pourcentage d'irbésartan (C25H28N6O) dans la portion d'irbésartan prise :
Résultat = (ru /rs ) × (Cs /Cu) × 100
ru = réponse maximale de l'irbésartan à partir de la solution échantillon
rs = réponse maximale de l'irbésartan à partir de la solution étalon
Cs = concentration d'USP Irbesartan RS dans la solution étalon (mg/mL)
Cu = concentration d'irbésartan dans la solution échantillon (mg/mL)
Critères d'acceptation : 98,0%-102,0% sur base anhydre
IMPURETÉS
• LIMITE D'AZIDE
Phase mobile : solution de soude 0,1 N
Solution mère étalon : 0,25 mg/mL d'azoture de sodium en phase mobile
Solution étalon : 0,312 µg/mL d'azoture de sodium en phase mobile, à partir de la solution mère étalon
Solution échantillon : 20 mg/mL d'Irbésartan en phase mobile
Système chromatographique
(Voir Chromatographie<621>, Adéquation du système.)
Mode : LC
Détecteur : conductimétrique avec une unité de suppression d'arrière-plan appropriée
Colonne : 4,0-mm × 25-cm ; Emballage L31
Débit : 1 mL/min
Volume d'injection : 200 µL
Adéquation du système
Échantillon : Solution étalon
Exigences d'aptitude
Rapport signal-sur-bruit : NLT 10 pour le pic azide
Analyse
Échantillons : solution standard et solution échantillon
Calculez la quantité d'azoture, en ppm, dans la portion d'irbésartan prise :
Résultat = (ru /rs) × (Cs/Cu) × (Mr1 /Mr2) × F
ru = surface du pic d'azoture de la solution échantillon
rs = aire du pic d'azoture de la solution étalon
Cs = concentration d'azoture de sodium dans la solution étalon (µg/mL)
Cu = concentration d'irbésartan dans la solution échantillon (mg/mL)
Mr1 = poids moléculaire de l'azoture, 42,02
Mr2 = poids moléculaire de l'azoture de sodium, 65,01
F = facteur de conversion d'unité, 1000
Critères d'acceptation : NMT 10 ppm
• IMPURETÉS ORGANIQUES
Phase tampon et mobile : préparez-vous comme indiqué dans le test.
Solution standard : Utiliser la solution d'adéquation du système, préparée comme indiqué dans le test.
Solution échantillon : 1 mg/mL d’irbésartan dans du méthanol
Système chromatographique
(Voir Chromatographie<621>, Adéquation du système.)
Mode : LC
Détecteur : UV 220 nm
Colonne : 4,0-mm × 25-cm ; emballage L1
Débit : 1 mL/min
Volume d'injection : 10 µL
Adéquation du système
Échantillon : Solution étalon
Exigences d'aptitude
Écart type relatif : NMT 2,0 %
Analyse
Échantillons : solution standard et solution échantillon
Calculez le pourcentage de composé A lié à l'irbésartan dans la portion d'irbésartan prise :
Résultat = (ru /rs ) × (Cs /Cu ) × 100
ru = réponse maximale du composé A lié à l'irbésartan à partir de la solution échantillon
rs = réponse maximale du composé A apparenté à l'irbésartan de la solution étalon
Cs = concentration du composé apparenté à l'irbésartan USP A RS dans la solution étalon (mg/mL)
Cu = concentration d'irbésartan dans la solution échantillon (mg/mL)
Calculez le pourcentage de toute autre impureté dans la portion d’irbésartan prise :
Résultat = (ru /rs ) × (Cs /Cu ) × 100
ru = réponse maximale de toute autre impureté de la solution échantillon
rs = réponse maximale de l'irbésartan à partir de la solution étalon
Cs = concentration d'USP Irbesartan RS dans la solution étalon (mg/mL)
Cu = concentration d'irbésartan dans la solution échantillon (mg/mL)
Critères d'acceptation
Composé A apparenté à l'irbésartan : NMT 0,2 %
Toute autre impureté : NMT 0,1 %
Impuretés totales : NMT 0,5 %
TESTS SPÉCIFIQUES
• DÉTERMINATION DE L'EAU, Méthode I<921> : NMT 0,5 %
EXIGENCES SUPPLÉMENTAIRES
• CONDITIONNEMENT ET CONSERVATION : Conserver dans des contenants hermétiques et conserver à une température inférieure à 30°.
• NORMES DE RÉFÉRENCE USP<11>
USP Irbésartan RS
USP Composé apparenté à l'irbésartan A RS
1-Acide pentanoylamino-cyclopentanecarboxylique [2′-(1H-tétrazol-5-yl)-biphényl-4-ylméthyl]-amide.
C25H30N6O 446,54