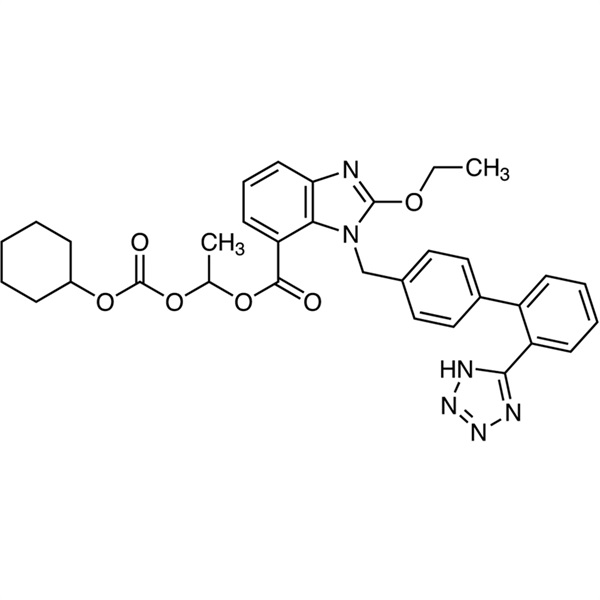
Norme API EP de l'analyse 99.0~101.0% de Candesartan Cilexetil CAS 145040-37-5
Ruifu Chemical est le principal fournisseur de candésartan cilexetil (CAS : 145040-37-5) de haute qualité, pouvant répondre à la norme EP. Ruifu fournit des API et des intermédiaires pharmaceutiques depuis plus de 15 ans.
Ruifu Chemical peut fournir une livraison dans le monde entier, des prix compétitifs et un excellent service.
Achetez du Candesartan Cilexetil et ses intermédiaires, veuillez nous contacter par e-mail : alvin@ruifuchem.com
Intermédiaire de Candesartan Cilexetil d'approvisionnement chimique de Ruifu avec la grande pureté
Candésartan Cilexétil CAS 145040-37-5
Candésartan CAS 139481-59-7
1-Carbonate de chloroéthylcyclohexyle CAS 99464-83-2
Ester éthylique intermédiaire C6 CAS 139481-41-7 de candésartan cilexétil
Candésartan Cilexétil Intermédiaire CAS 139481-44-0
Trityl Candésartan Cilexétil CAS 170791-09-0
| Nom chimique | Candésartan Cilexétil |
| Synonymes | TCV-116 ; 1-(((Cyclohexyloxy)carbonyl)oxy)éthyle 1-((2'-(1H-tétrazol-5-yl)-[1,1'-biphényl]-4-yl)méthyl)-2-éthoxy-1H-benzo[d]imidazole-7-Carboxylate |
| Numéro CAS | 145040-37-5 |
| État des stocks | En stock, production pouvant atteindre des tonnes |
| Formule moléculaire | C33H34N6O6 |
| Poids moléculaire | 610.66 |
| Densité | 1,37 ± 0,10 g/cm3 |
| Point de fusion | 168,0-170,0℃ |
| Certificat d'authenticité et fiche signalétique | Disponible |
| Conditions de stockage | 2-8℃ |
| Sensible | Sensible à la chaleur |
| Origine du produit | Shanghai, Chine |
| Catégories de produits | API (Ingrédient Pharmaceutique Actif) |
| Marque | Produit chimique Ruifu |
| Articles | Spécifications | Résultats |
| Apparence | Poudre blanche ou presque blanche | Poudre blanche |
| Identification-RI | Conforme au spectre de référence | Conforme |
| Identification- UV | Absorptions maximales à 254 nm, absorption minimale à 242 nm | Conforme |
| Eau (K.F) | ≤0,30% | 0,19% |
| Solvants résiduels | ||
| Méthanol | ≤3000ppm | Non détecté |
| Éthanol | ≤5000ppm | Non détecté |
| Éther éthylique | ≤5000ppm | 62 ppm |
| Acétone | ≤5000ppm | 505 ppm |
| Acétate d'éthyle | ≤5000ppm | Non détecté |
| Dichlorométhane | ≤600 ppm | Non détecté |
| Diméthylformamide | ≤880 ppm | Non détecté |
| Substances associées | ||
| Impureté A | ≤0,15% | 0,04% |
| Impureté B | ≤0,30% | 0,03% |
| Impureté F | ≤0,20% | 0,02% |
| Impureté G | ≤0,20% | 0,04% |
| Impureté H | ≤0,15% | Non détecté |
| Autre impureté individuelle | ≤0,10 % | 0,04% |
| Impuretés totales | ≤0,60% | 0,23% |
| Cendres sulfatées | ≤0,10 % | 0,07% |
| Métaux lourds | ≤10 ppm | <10 ppm |
| Dosage (substance séchée) | 99,0~101,0 % | 99,9% |
| Norme de test | Norme PE | Conforme |
Forfait : Bouteille, sac en papier d'aluminium, fût de 25 kg/carton ou selon les exigences du client.
Conditions de stockage : Gardez le récipient bien fermé. Conserver dans un entrepôt frais, sec (2-8℃) et bien ventilé, à l'écart des substances incompatibles. Tenir à l'écart du soleil ; éviter le feu et les sources de chaleur ; éviter l'humidité.
Expédition : Livrez dans le monde entier par avion, par mer, par FedEx / DHL Express. Fournir une livraison rapide et fiable.

Codes de risque
R20/21/22 - Nocif par inhalation, par contact avec la peau et par ingestion.
R36/37/38 - Irritant pour les yeux, les voies respiratoires et la peau.
R50 - Très toxique pour les organismes aquatiques
R48/20 -
R61 - Peut nuire à l'enfant à naître
Description de la sécurité
S26 - En cas de contact avec les yeux, rincer immédiatement et abondamment à l'eau et consulter un médecin.
S36 - Portez des vêtements de protection appropriés.
S61 - Éviter le rejet dans l'environnement. Se référer aux instructions spéciales/fiches de données de sécurité.
S45 - En cas d'accident ou de malaise, consulter immédiatement un médecin (si possible lui montrer l'étiquette).
S53 - Éviter l'exposition - obtenir des instructions spéciales avant utilisation.
WGK Allemagne 3
RTECSDD6672500
Code SH 2933990099
Le candésartan cilexétil (TCV - 116) (CAS : 145040 - 37 - 5) est un antagoniste des récepteurs de l'angiotensine II avec une CI50 de 0,26 nM, utilisé dans le traitement de l'hypertension. Le candésartan est un bloqueur des récepteurs de l'angiotensine (ARA) qui peut être utilisé seul ou avec d'autres agents pour traiter l'hypertension. Il est administré par voie orale sous forme de promédicament, le candésartan cilexétil, qui est rapidement converti en son métabolite actif, le candésartan, lors de son absorption dans le tractus gastro-intestinal. Le candésartan abaisse la tension artérielle en antagonisant le système rénine-angiotensine-aldostérone (RAAS) ; il entre en compétition avec l'angiotensine II pour se lier au sous-type du récepteur de l'angiotensine II de type - 1 (AT1) et empêche les effets d'augmentation de la pression artérielle de l'angiotensine II. Contrairement aux inhibiteurs de l’enzyme de conversion de l’angiotensine (ECA), les ARA n’ont pas l’effet indésirable d’une toux sèche. Le candésartan peut être utilisé pour traiter l'hypertension, l'hypertension systolique isolée, l'hypertrophie ventriculaire gauche et la néphropathie diabétique. Il peut également être utilisé comme agent alternatif pour le traitement de l'insuffisance cardiaque, du dysfonctionnement systolique, de l'infarctus du myocarde et de la maladie coronarienne.
CANDESARTAN CILEXÉTIL
Candésartan cilexétili
C33H34N6O6 Monsieur 611
[145040-37-5]
DÉFINITION
(1RS)-1-[[(Cyclhexyloxy)carbonyl]oxy]éthyle
2-éthoxy-1-[[2′-(1H-tétrazol-5-yl)biphényl-4-yl]méthyl]-1H-benzimidazole-7-carboxylate.
Contenu : 99,0 pour cent à 101,0 pour cent (substance anhydre).
FABRICATION
Les N-nitrosamines étant classées comme cancérogènes probables pour l'homme, leur présence dans le candésartan cilexétil doit être évitée ou limitée autant que possible. Pour cette raison, les fabricants de candésartan cilexétil à usage humain doivent procéder à une évaluation du risque de formation et de contamination de N-nitrosamine au cours de leur processus de fabrication ; si cette évaluation identifie un risque potentiel, le processus de fabrication doit être modifié pour minimiser la contamination et une stratégie de contrôle doit être mise en œuvre pour détecter et contrôler les impuretés de N-nitrosamine dans le candésartan cilexétil. Le chapitre général 2.5.42. Les N-Nitrosamines contenues dans les substances actives sont disponibles pour aider les fabricants.
PERSONNAGES
Aspect : poudre blanche ou presque blanche.
Solubilité : pratiquement insoluble dans l'eau, librement soluble dans le chlorure de méthylène et légèrement soluble dans l'éthanol anhydre.
Il montre un polymorphisme (5.9).
IDENTIFICATION
Spectrophotométrie d'absorption infrarouge (2.2.24).
Comparaison : candésartan cilexétil CRS.
Si les spectres obtenus présentent des différences, dissoudre séparément la substance à examiner et la substance de référence dans de l'éthanol R anhydre, évaporer à sec et enregistrer de nouveaux spectres en utilisant les résidus.
ESSAIS
Substances apparentées. Chromatographie liquide (2.2.29). Préparez les solutions immédiatement avant utilisation.
Mélange de solvants : eau R, acétonitrile R (40:60 V/V).
Solution d’essai. Dissoudre 20 mg de la substance à examiner dans 50,0 mL du mélange de solvants.
Solution de référence (a). Diluer 1,0 mL de la solution de test à 100,0 mL avec le mélange de solvants. Diluer 1,0 mL de cette solution à 10,0 mL avec le mélange de solvants.
Solution de référence (b). Dissoudre 5 mg de candésartan cilexétil pour vérifier l'adéquation du système CRS (contenant les impuretés A, B et F) dans le mélange de solvants et diluer à 10 mL avec le mélange de solvants.
Solution de référence (c). Dissoudre 2,5 mg de candésartan cilexétil pour l'identification du pic CRS (contenant les impuretés G et H) dans le mélange de solvants et diluer à 5 mL avec le mélange de solvants.
Colonne :
- taille : l = 0,15 m, Ø = 3,9 mm ;
- phase stationnaire : gel de silice octadécylsilyl coiffé pour
chromatographie R (4 μm).
Phase mobile :
- phase mobile A : acide acétique glacial R, eau pour
chromatographie R, acétonitrile R (1:43:57 V/V/V) ;
- phase mobile B : acide acétique glacial R, eau pour
chromatographie R, acétonitrile R (1:10:90 V/V/V) ;
Durée (min) Phase mobile A (pourcentage V/V) Phase mobile B (pourcentage V/V)
0 - 3 100 0
3 - 33 100 → 0 0 → 100
33 - 40 0 100
Débit : 0,8 mL/min.
Détection : spectrophotomètre à 254 nm.
Injection : 10 μL.
Identification des impuretés : utiliser le chromatogramme fourni avec le candésartan cilexétil pour l'adéquation du système CRS et le chromatogramme obtenu avec la solution de référence (b) pour identifier les pics dus aux impuretés A, B et F ; utiliser le chromatogramme fourni avec le candésartan cilexétil pour l'identification des pics CRS et le chromatogramme obtenu avec la solution de référence (c) pour identifier les pics dus aux impuretés G et H.
Rétention relative par rapport au candésartan cilexétil
(temps de rétention = environ 11 min) : impureté G = environ 0,2 ;
impureté A = environ 0,4 ; impureté B = environ 0,5 ;
impureté F = environ 2,0 ; impureté H = environ 3,5.
Adéquation du système : solution de référence (b) :
- résolution : minimum 4,0 entre les pics dus aux impuretés A et B.
Limites :
- facteurs de correction : pour le calcul de la teneur, multiplier les surfaces de pic des impuretés suivantes par le facteur de correction correspondant : impuretés A et G = 0,7 ;
impureté H = 1,6 ;
- impureté B : pas plus de 3 fois la surface du pic principal dans le chromatogramme obtenu avec la solution de référence (a) (0,3 pour cent) ;
- impuretés F, G : pour chaque impureté, pas plus de deux fois la surface du pic principal dans le chromatogramme obtenu avec la solution témoin (a) (0,2 pour cent) ;
- impuretés A, H : pour chaque impureté, pas plus de 1,5 fois la surface du pic principal du chromatogramme obtenu avec la solution témoin (a) (0,15 pour cent) ;
- impuretés non précisées : pour chaque impureté, pas plus que la surface du pic principal dans le chromatogramme obtenu avec la solution témoin (a) (0,10 pour cent) ;
- total : pas plus de 6 fois la surface du pic principal du chromatogramme obtenu avec la solution de référence (a) (0,6 pour cent) ;
- limite de non-respect : 0,5 fois la surface du pic principal dans le chromatogramme obtenu avec la solution de référence (a) (0,05 pour cent).
Eau (2.5.32) : maximum 0,3 pour cent, déterminé sur 60,0 mg.
Cendres sulfatées (2.4.14) : maximum 0,1 pour cent, déterminé sur 1,0 g.
ESSAI
Dissoudre 0,500 g dans 60 mL d'acide acétique glacial R. Titrer immédiatement avec de l'acide perchlorique 0,1 M en déterminant le point final par potentiométrie (2.2.20) au 1er point d'inflexion.
1 mL d'acide perchlorique 0,1 M équivaut à 61,1 mg de C33H34N6O6.
IMPURETÉS
Impuretés spécifiées : A, B, F, G, H.
Autres impuretés détectables (les substances suivantes, si elles sont présentes en quantité suffisante, seraient détectées par l'un ou l'autre des tests de la monographie. Elles sont limitées par le critère général d'acceptation pour les impuretés autres/non spécifiées et/ou par la monographie générale Substances à usage pharmaceutique (2034). Il n'est donc pas nécessaire d'identifier ces impuretés pour démontrer la conformité. Voir également 5.10. Contrôle des impuretés dans les substances à usage pharmaceutique) : C, D, E, I.
A. éthyle 2-éthoxy-1-[[2′-(1H-tétrazol-5-yl)biphényl-4-yl]méthyl]-1H-benzimidazole-7-carboxylate,
B. (1RS)-1-[[(cyclohexyloxy)carbonyl]oxy]éthyl 2-oxo-3-[[2′-(1H-tétrazol-5-yl)biphényl-4-yl]méthyl]-2,3-dihydro-1H-benzimidazole-4-carboxylate,
C. (1RS)-1-[[(cyclohexyloxy)carbonyl]oxy]éthyl 3-[[2′-(1-éthyl-1H-tétrazol-5-yl)biphényl-4-yl]méthyl]-2-oxo-2,3-dihydro-1H-benzimidazole-4-carboxylate,
D. (1RS)-1-[[(cyclohexyloxy)carbonyl]oxy]éthyl 3-[[2′-(2-éthyl-2H-tétrazol-5-yl)biphényl-4-yl]méthyl]-2-oxo-2,3-dihydro-1H-benzimidazole-4-carboxylate,
E. (1RS)-1-[[(cyclohexyloxy)carbonyl]oxy]éthyl 2-éthoxy-1-[[2′-(1-éthyl-1H-tétrazol-5-yl)biphényl-4-yl]méthyl]-1H-benzimidazole-7-carboxylate,
F. (1RS)-1-[[(cyclohexyloxy)carbonyl]oxy]éthyl 2-éthoxy-1-[[2′-(2-éthyl-2H-tétrazol-5-yl)biphényl-4-yl]méthyl]-1H-benzimidazole-7-carboxylate,
G. 2-éthoxy-1-[[2′-(1H-tétrazol-5-yl)biphényl-4-yl]méthyl]-1H-benzimidazole-7-acide carboxylique (candésartan),
H. (1RS)-1-[[(cyclohexyloxy)carbonyl]oxy]éthyl 2-éthoxy-1-[[2′-[1-(triphénylméthyl)-1H-tétrazol-5-yl]biphényl-4-yl]méthyl]-1H-benzimidazole-7-carboxylate
(N-tritylcandésartan),
I. méthyle 2-éthoxy-1-[[2′-(1H-tétrazol-5-yl)biphényl-4-yl]méthyl]-1H-benzimidazole-7-carboxylate.