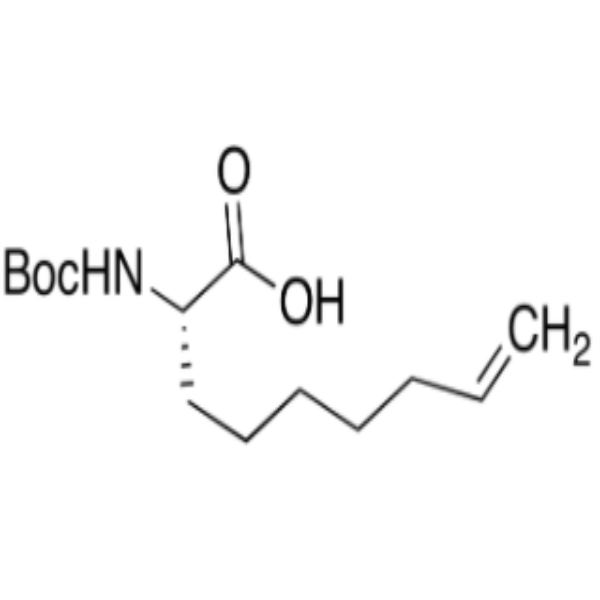
(S)-2-(Boc-Amino)non-8-Acide énoïque CAS 300831-21-4 Pureté >98,0 % (GC) e.e >99,0 % Usine intermédiaire de paritaprévir
Shanghai Ruifu Chemical Co., Ltd. est le principal fabricant et fournisseur d'acide (S)-2-(Boc-Amino)non-8-Enoic (CAS : 300831-21-4) avec une production commerciale de haute qualité. Ruifu Chemical propose une large gamme de composés chiraux. Nous pouvons fournir un certificat d'analyse (COA), une livraison dans le monde entier, des quantités petites et en vrac disponibles. Veuillez contacter : alvin@ruifuchem.com
| Nom chimique | (S)-2-(Boc-Amino)non-8-Acide énoïque |
| Synonymes | (S)-2-(tert-Butoxycarbonylamino)non-8-Acide énoïque ; (S)-2-(Boc-Amino)-8-Acide nonénoïque ; (2S)-2-[(2-Méthylpropan-2-yl)oxycarbonylamino]non-8-Acide énoïque ; (2S)-2-{[(tert-Butoxy)carbonyl]amino}non-8-Acide énoïque |
| Numéro CAS | 300831-21-4 |
| Numéro CAT | RF-CC347 |
| État des stocks | En stock |
| Formule moléculaire | C14H25NO4 |
| Poids moléculaire | 271,35 |
| Densité | 1,035 ± 0,06 g/cm3 |
| Marque | Produit chimique Ruifu |
| Article | Spécifications |
| Apparence | Liquide marron |
| Pureté / Méthode d'analyse | >98,0 % (GC) |
| e.e | >99,0% |
| Norme de test | Norme d'entreprise |
| Utilisation | Intermédiaires du Paritaprévir (CAS : 1216941-48-8) |
Forfait: Bouteille fluorée, 25 kg/fût ou selon les exigences du client
Conditions de stockage :Conserver dans des récipients scellés dans un endroit frais et sec ; Protéger de la lumière et de l'humidité


L'acide (S)-2-(Boc-Amino)non-8-Enoic (CAS : 300831-21-4) peut être utilisé comme intermédiaire dans la synthèse du paritaprévir (CAS : 1216941-48-8) et des analogues associés. Le paritaprévir est un inhibiteur de protéase NS3/4A de deuxième génération et est un composant de la thérapie combinée entièrement orale et sans interféron contre le virus de l'hépatite C développée par Enanta Pharmaceuticals et AbbVie. Le comprimé à dose fixe de Paritaprévir, Ombitasvir et Ritonavir pris en association avec le Dasabuvir a été approuvé pour le traitement du génotype 1 chronique du VHC aux États-Unis et dans l'UE en 2014, et a ensuite été approuvé pour le traitement de l'infection chronique par le VHC de génotype 4 sans cirrhose par la FDA américaine en 2015.